Paciente de 74 años, con el diagnóstico indicado. Hace un año presentaba este ECG
El ECG actual es este
¿Qué dispositivo más probable se le ha colocado a este paciente?

Como muchos habéis adivinado se trata de un ECG típico de síndrome de Wolf-Parkinson-White. Los criterios diagnósticos son:
a) Intervalo PR corto (<0,12 segundos)
b) Onda delta
c) Compleo QRS ensanchado
Como sabéis en este síndrome existe una vía anómala de conducción, el haz de Kent, que conecta la aurícula con el tejido muscular de los ventrículos. Esta vía anómala suele conducir el estímulo de forma más rápida que el nódulo auriculoventricular. Por esto se acorta el intervalo PR. El estímulo conducido a través de la vía anómala llega al miocardio ventricular (generalmente termina en el tejido muscular). Esto da lugar a la denominada onda delta, que inicia el complejo QRS. Mientras tanto, el estímulo que se propaga a través del nódulo auriculoventricular llega al ventrículo y comienza a conducirse a través del tejido específico de conducción, despolarizando el resto de miocardio. En definitiva, el complejo QRS empieza antes y termina como lo hace normalmente, lo que explica que el QRS esté ensanchado.
Otra cosa apasionante para los entusiastas de las arritmias es saber localizar la via viendo el ECG. He encontrado un algoritmo muy sencillo que estoy elaborando y que se inicia viendo si la onda delta es positiva o negativa en V1. Cuando lo tenga presentable os lo colgaré.
Desde el punto de vista del médico de Atención Primaria es importante el diagnóstico electrocardiográfico para enviar estos pacientes a la consulta del cardiólogo. Sabéis que estos pacientes pueden estar asintomáticos pero pueden referir palpitaciones por presentar episodiso de taquicardias supraventriculares, o fibrilación auricular. Incluso la muerte súbita puede ser también una forma de debut de la enfermedad.
El estudio en fase III PARADIGM-HF analiza la eficacia del LCZ696, el primero de una nueva clase farmacológica denominada “Angiotensin Receptor Neprilysin Inhibitor (ARNI)”. El estudio PARADIGM-HF ha sido detenido prematuramente en un análisis intermedio al demostrar una disminución estadísticamente significativa de la mortalidad cardiovascular en comparación con el mejor tratamiento actual, los IECAs.
El estudio PARADIGM-HF compara este nuevo fármaco LCZ696 (inhibidor del receptor angiotensina-neprilisin) con enalapril en el tratamiento de pacientes con insuficiencia cardiaca (NYHA II-IV) con fracción de eyección reducida, para evaluar su capacidad de reducción de un compuesto de muerte por causas cardiovasculares o hospitalización.
Los autores de este estudio partían de que en investigaciones previas el enalapril mejoraba la supervivencia en pacientes con insuficiencia cardiaca con fracción de eyección reducida.
La metodología planteada fue la siguiente: ensayo doble ciego donde se aleatorizaron 8.442 pacientes con insufiencia cardiaca de clase II,III o IV y una fracción de eyección de 40% o menos, a recibir o bien LCZ696 (a una dosis de 200 mg dos veces al día) o enalapril (a una dosis de 10 mg dos veces al día), junto con la terapia que se recomienda actualmente en estos pacientes. El objetivo primario fue un compuesto de muerte por causas cardiovasculares o hospitalización por insufiencia cardiaca, pero el ensayo estaba diseñado para detectar la diferencia en las tasas de muerte por causa cardiovascular.
Los resultados comunicados fueron los siguientes: el ensayo se tuvo que detener prematuramente, de acuerdo a reglas preespecificadas, tras una mediana de seguimiento de 27 meses, porque el límite para un beneficio extremadamente claro con LCZ696 se había superado. En el momento del cierre del estudio, el objetivo primario había ocurrido en 914 pacientes (21,8%) en el grupo LCZ696, y 1.117 pacientes (26,5%) en el grupo de enalapril (hazard ratio en el grupo LCZ696 0,80; intervalo de confianza [IC] 95% 0,73-0,87; P<0,001). Un total de 771 pacientes (17,0%) que recibieron LCZ696 y 835 pacientes (19,8%) que recibieron enalapril murieron (hazard ratio para muerte por cualquier causa 0,84; IC 95% 0,76-0,93; P<0,001); de estos pacientes, 558 (13,3%) y 693 (16,5%) respectivamente, murieron por causas cardiovasculares (hazard ratio 0,80; IC95% 0,71-0,89; P<0,001). Si se comparaba con enalapril, LCZ696 también redujo el riesgo de hospitalización por insuficiencia cardiaca por 21% (P<0,001) y disminuyó los síntomas y las limitaciones físicas por insuficiencia cardiaca (P=0,001). El grupo de LCZ696 tuvo mayores proporciones de pacientes con hipotensión y angioedema no importante, pero menores proporciones de empeoramiento renal, hiperpotasemia y tos, en comparación con el grupo de enalapril.
Ante estos resultados los autores concluyeron que el LCZ696 fue superior al enalapril en la reducción del riesgo de muerte y de hospitalización por insuficiencia cardiaca.
Aquí os dejo la referencia
Seria bueno que todos leyerais este artículo y os fuerais haciendo una idea en vuestra cabeza.
Todos sabéis que cuando comienza a ver la luz un fármaco tan exitoso como parece este, hay que ser muy cautos a la hora de interpretar los resultados y estar un poco expectantes para ver por donde van los tiros.
Yo prometo manteneros al día….
En caso de que el infarto haya sido tan extenso que afecte la función del ventrículo izquierdo con disfunción ventricular no queda duda de que es OBLIGADO utilizar los IECAs y determinados betabloqueantes de los que luego hablaremos. También hay bases para utilizar la eplerenona. En algunas ocasiones diuréticos.
Hablando de los BETABLOQUEANTES, en cuanto a la aparición de insuficiencia cardiaca después de un IAM, en el Carvedilol Post Infarct Survival Control in Left Ventricular Dysfunction, en el que se incluyeron pacientes en los 2-21 días tras el IAM, con fracción de eyección de ventrículo izquierdo reducida y tratamiento óptimo, la mortalidad por todas las causas fue inferior en el grupo de betabloqueantes que en el grupo placebo (el 12 frente al 15%) En el estudio CIBIS II (Cardiac Insuffi¬ciency Bisoprolol Study II), la causa más frecuente de insuficiencia cardiaca entre los participantes fue la cardiopatía isquémica (49,9%) y la fracción de eyección del ventrículo izquierdo promedio fue del 27,7%; en este estudio bisoprolol disminuyó la mortalidad total en pacientes con insuficiencia cardiaca por disfunción sistólica, así como también el número de reingresos hospitalarios por empeoramiento de la insuficiencia cardiaca. Estos efectos beneficiosos se observaron en pacientes ya tratados con diuréticos e IECAs y ocurrieron independientemente de cual fuera la causa primaria de la disfunción sistólica.
Desde un punto de vista práctico si el paciente ha debutado con IC introducimos el bisoprolol a dosis bajísimas y muy poco a poco… en cuanto se pueda, refiriendome a que el paciente no esté en el momento más agudo. La experiencia me dice que puede ser ya a las 48 h. A lo largo de los dias del ingreso intentamos ir subiendo más la dosis hasta la máxima tolerancia.
El estudio EPHESUS ha apoyado el uso de la EPLERENONA. Se aleatorizaron a 6.642 pacientes post- IAMCEST con disfunción VI (fracción de eyección < 40%) e insuficiencia cardiaca o diabetes, a recibir eplerenona, un antagonista selectivo de la aldosterona, o placebo. Tras un seguimiento medio de 16 meses hubo una reducción relativa del 15% en la mortalidad total y una reducción del 13% en la variable combinada de muerte y hospitalización por episodios cardiovasculares. La hiperpotasemia importante fue más frecuente en el grupo que recibió eplerenona. Los resultados sugieren que la inhibición de la aldosterona puede considerarse en pacientes con IAMCEST que tengan una fracción de eyección ≤ 40% e insuficiencia cardiaca o diabetes, siempre que la concentración de creatinina sea < 221 mmol/l (2,5 mg/dl) en los varones y < 177 mmol/l (2,0 mg/dl) en las mujeres, y que el potasio sea < 5,0 mEq/l. Es necesario realizar una monitorización de rutina del potasio sérico.
Por tanto y ya uniendo todo el paciente del IAM del caso 2 se fue de alta con el siguiente tratamiento
– CLOPIDOGREL 75 MG 1 comprimido CADA 24 HORAS – DESAYUNO.
– ACETILSALICILICO ACIDO 100 MG – COMIDA.
Debe mantener esta medicación al menos un año. No puede ser suspendida sin indicación del cardiólogo.
– FUROSEMIDA 40 MG COMP – 1/2 comprimido CADA 24 HORAS- DESAYUNO
– ENALAPRIL 2,5 MG 1 comprimido CADA 24 HORAS -DESAYUNO-
– BISOPROLOL 2,5 MG -1 comprimido en DESAYUNO y otro en CENA
– EPLERENONA 25 MG CADA 24 HORAS DESAYUNO
– ATORVASTATINA 40 MG 1 comprimido en CENA.
– PANTOPRAZOL 40 MG AYUNAS
– ENOXAPARINA 40 MG: 1 INYECCIÓN SUBCUTÁNEA A LAS 17 H DIARIA previo a paso a Sintrom.
El otro día una residente muy sagaz me dijo: “Pues yo creo que en Cardiologia se emplean cuatro o cinco clases de fármacos en la mayoría de los pacientes”… Y tiene razón. Yo pienso que el arte del cardiólogo está en saberlos combinar.
En el caso que nos ocupa, en general, un paciente tras un infarto agudo de miocardio se irá de alta con doble antiagregación, hipolipemiantes y betabloqueantes. Casi siempre con IECAs. Alguna vez con inhibidores de la aldosterona o diuréticos. Excepcionalmente con antagonistas de calcio. Y yo diría que en la epoca actual casi excepcionalmente con nitratos.
Se debe usar ASPIRINA de forma indefinida en todos los pacientes con IAMCEST. Las dosis de aspirina que deben emplearse es un tema debatido. Pero para el tratamiento a largo plazo se suelen utilizar las dosis bajas (70-100 mg).
La DOBLE antiagregación plaquetaria, que combina aspirina y un inhibidor del receptor de ADP (clopidogrel, prasugrel o ticagrelor), en pacientes con IAMCEST que se sometan a angioplastia primaria (hasta 12 meses), fibrinolisis (hasta 12 meses, aunque los datos disponibles corresponden sólo a 1 mes de doble antiagregación plaquetaria) y en pacientes que no hayan recibido tratamiento de reperfusión (durante, por los menos, 1 mes y hasta 12 meses). ****La elección del fármaco inhibidor del receptor de ADP se discutirá en otro post.
Respecto a la duración de la doble antiagregación nosotros en general recomendamos un año, pero en sentido estricto, suponeros que hubiera que realizar una cirugía, lo minimo es 1 mes en pacientes portadores de un stent convencional y 6 meses para aquellos con stent farmacoactivo.
Es importante informar a los pacientes y a sus médicos de la necesidad de evitar la interrupción prematura de la doble antiagregación plaquetaria. Por eso en el informe de alta siempre añadimos una coletilla en este sentido.
Los beneficios de las ESTATINAS en la prevención secundaria se han demostrado de forma inequívoca; varios estudios clínicos específicos han establecido el beneficio de iniciar un tratamiento con estatinas de forma precoz e intensiva. Los estudios clínicos favorecen la administración de atorvastatina a dosis de 80 mg diarios.
Sobre los BETABLOQUEANTES os diré que es un poco el caso de “coge fama y echate a dormir” El beneficio del tratamiento a largo plazo con bloqueadores beta tras un IAMCEST está bien establecido, aunque la mayor parte de los datos proceden de estudios previos a la era moderna del tratamiento de reperfusión y la farmacoterapia. En los estudios contemporáneos que utilizan angioplastia primaria, los bloqueadores beta todavía no se han investigado; aunque parece razonable extrapolar sus beneficios a este contexto. Normalmente a los cardiólogos nos gustan los betabloqueantes. Digamos que nos dan seguridad. Si la fracción de eyección es buena los pacientes suelen ser dados de alta con Atenolol. Ya hablaremos de otras excepciones.
Respecto a los IECAs como observáis he puesto casi siempre. Está bien establecido que los IECA deben administrarse a pacientes con fracción de eyección deprimida (< 40%) o a los que han tenido insuficiencia cardiaca en la fase inicial. Una revisión sistemática de los estudios que han utilizado IECA de forma precoz en pacientes con IAMCEST ha indicado que este tratamiento es seguro, bien tolerado y se asocia a una reducción pequeña pero significativa de la mortalidad a los 30 días, produciéndose la mayor parte del beneficio en la primera semana. Las opiniones siguen siendo divergentes sobre si hay que administrar IECA a todos los pacientes o sólo a los de alto riesgo.
Se debe considerar el uso de IECA en todos los pacientes con aterosclerosis pero, teniendo en cuenta el efecto relativamente modesto que tienen, su uso a largo plazo no puede considerarse obligatorio en pacientes post-IAMCEST normotensos, sin insuficiencia cardiaca o que no tengan disfunción VI o diabetes.
Por tanto, el caso más sencillo, POR PONER UN EJEMPLO, se trataria de un paciente con IAMCEST inferior con angioplastia primaria colocándose un stent en CD, normotenso y con buena función ventricular. Al alta
– Adiro 100
– Clopidogrel vs Prasugrel vs Ticagrelor
– Atorvastatina 80
– Atenolol 50 …. Casi seguro.
Imaginaros que este paciente fuera hipertenso, pues se iria con un IECA. En caso de intolerancia a IECA utilizaríamos ARA II.
¿Habéis visto que fácil? … Pues rizaremos el rizo en el siguiente post.
Buenas noches…
Esta es la pregunta que me hizo el residente cuando actualizamos el tratamiento del paciente después de conocer la existencia del trombo.
Y la respuesta es si.
Francisco, el paciente de 75 años estaba con doble antiagregación tras el intervencionismo coronario urgente con Aspirina 100 mg y Ticagrelor 90 mg/12 h. (este ultimo uno de los nuevos antiagregantes)
Cuando en el ecocardiograma se objetivó el trombo mural comenzamos tratamiento con Enoxaparina a dosis anticoagulantes (para después pasar a Sintrom).
En este momento también cambiamos el Ticagrelor por Clopidogrel 75 mg, puesto que con los nuevos antiagregantes no hay suficiente experiencia con el uso de doble antiagregación y anticoagulación.
Por tanto al alta Francisco se fue con doble antiagregación y anticoagulación.
COMENTARIO
Hay consenso en que los trombos murales, una vez que se diagnostican, requieren tratamiento anticoagulante oral con antagonistas de la vitamina K durante 6meses. Sin embargo, esta opinión no se ha revisado en la era de los stents y la doble antiagregación plaquetaria. La combinación de anticoagulación y doble antiagregación plaquetaria
en una terapia triple aumenta el riesgo hemorrágico. La duración óptima de un tratamiento antitrombótico triple de este tipo no se conoce y deben tenerse
en cuenta los riesgos relativos de hemorragia y la trombosis intra-stent.
La repetición de las técnicas de imagen del VI después de 3meses de tratamiento
Puede permitir la interrupción de la anticoagulación antes de los 6 meses si hay evidencia de que el trombo ha desaparecido, sobre todo si se ha producido recuperación
de la motilidad de la pared apical. (Guía de práctica clínica de la Sociedad Europea de Cardiologia para el manejo del infarto agudo de miocardio en pacientes con elevación del segmento ST, 2013)
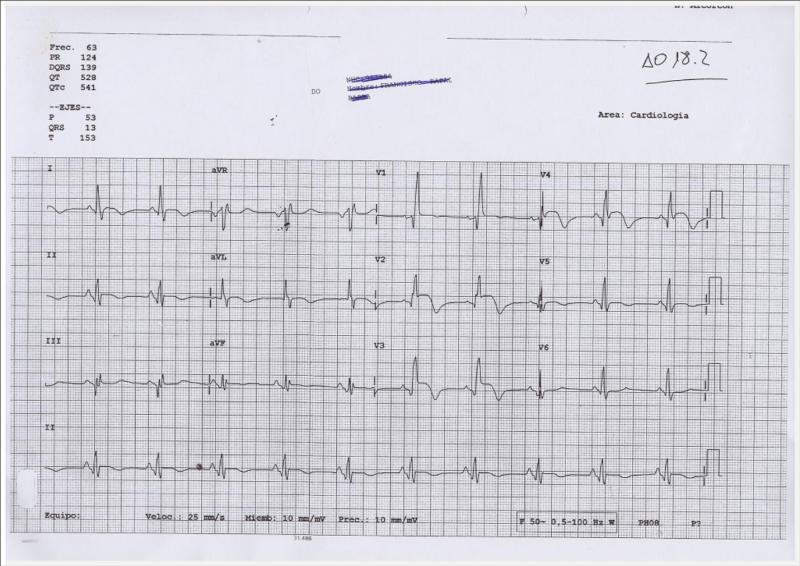
Este es un ECG que los cardiólogos diríamos por una parte que es muy bonito y por otra que es muy feo Muy bonito porque hay varios hallazgos muy destacables en cuanto a su descripción y muy feo por lo que puede implicar en el pronóstico de este paciente.
En este ECG, al alta del paciente, como ya dijimos, se muestran unas ondas Q de V1 a V4, signo de un infarto anterior extenso. Además en esas mismas derivaciones el patrón es qR, y esta R es en realidad la segunda R o R’ de un Bloqueo de Rama Derecha (y por tanto ha perdido la 1ª R) Además se observa una persistencia de la elevación del segmento ST. Y finalmente también parecen unas ondas Q en II, III y avF.
La persistencia de la elevación del ST al alta hospitalaria puede ser considerado estar asociado con un infarto de gran tamaño y en 30% de los casos con formación de un aneurisma del VI. Os dejo una cita de un articulo relativamente reciente al respecto (1) de algo que ya esta descrito hace muchos años.
Pues efectivamente este paciente ingresó por un Síndrome Coronario Agudo con Elevación del ST al que se hizo una Coronariografia urgente que mostró una oclusión aguda de la Descendente Anterior (DA) media y una postero-lateral (que es una rama de la CD) con una lesión severa.Se realizó una revascularización percutánea con stent farmacoactivo en DA media
El ecocardiograma al alta mostró:
VI NO DILATADO CON DISFUNCION SISTOLICA MODERADA ( 40% ) con acinesia de la mitad distal de cara anterior, dos tercios distales de SIV . Discinesia del apex afectando al tercio distal de todas las caras. Ademas necrosis establecida del talon infero y posterobasal . Además una imagen de TROMBO APICAL
¿Os dais cuenta de cuanta información nos puede dar un ECG?
Por todo lo que os he dicho anteriormente, entendereis que el ECG del caso 2 es MUY BONITO Y MUY FEO a la vez.
Ya trataremos mas adelanta el diagnóstico del IAM en presencia de bloqueo de rama, que ya se que esto da muchos quebraderos de cabeza.
1. Galiuto L(1), Barchetta S, Paladini S, Lanza G, Rebuzzi AG, Marzilli M, Crea F. Functional and structural correlates of persistent ST elevation after acute myocardial infarction successfully treated by percutaneous coronary intervention. Heart. 2007 Nov;93(11):1376-80. Epub 2007 Feb 19.