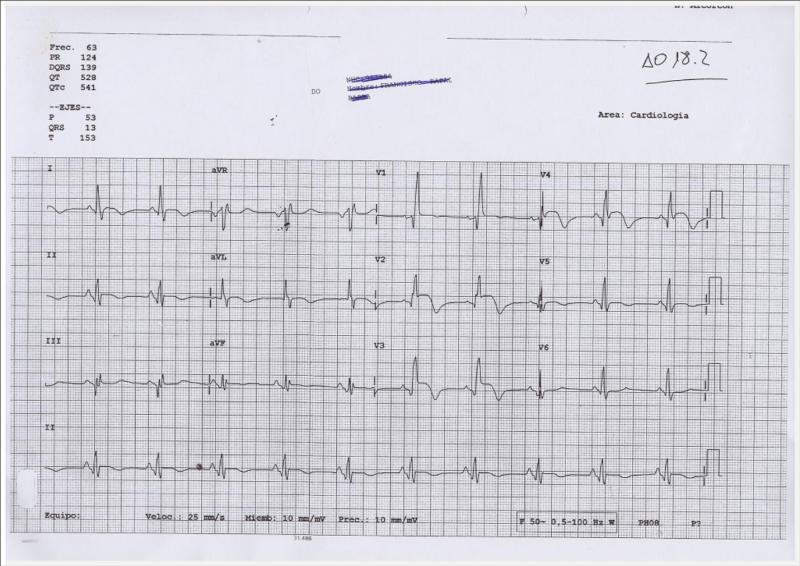
Este es un ECG que los cardiólogos diríamos por una parte que es muy bonito y por otra que es muy feo Muy bonito porque hay varios hallazgos muy destacables en cuanto a su descripción y muy feo por lo que puede implicar en el pronóstico de este paciente.
En este ECG, al alta del paciente, como ya dijimos, se muestran unas ondas Q de V1 a V4, signo de un infarto anterior extenso. Además en esas mismas derivaciones el patrón es qR, y esta R es en realidad la segunda R o R’ de un Bloqueo de Rama Derecha (y por tanto ha perdido la 1ª R) Además se observa una persistencia de la elevación del segmento ST. Y finalmente también parecen unas ondas Q en II, III y avF.
La persistencia de la elevación del ST al alta hospitalaria puede ser considerado estar asociado con un infarto de gran tamaño y en 30% de los casos con formación de un aneurisma del VI. Os dejo una cita de un articulo relativamente reciente al respecto (1) de algo que ya esta descrito hace muchos años.
Pues efectivamente este paciente ingresó por un Síndrome Coronario Agudo con Elevación del ST al que se hizo una Coronariografia urgente que mostró una oclusión aguda de la Descendente Anterior (DA) media y una postero-lateral (que es una rama de la CD) con una lesión severa.Se realizó una revascularización percutánea con stent farmacoactivo en DA media
El ecocardiograma al alta mostró:
VI NO DILATADO CON DISFUNCION SISTOLICA MODERADA ( 40% ) con acinesia de la mitad distal de cara anterior, dos tercios distales de SIV . Discinesia del apex afectando al tercio distal de todas las caras. Ademas necrosis establecida del talon infero y posterobasal . Además una imagen de TROMBO APICAL
¿Os dais cuenta de cuanta información nos puede dar un ECG?
Por todo lo que os he dicho anteriormente, entendereis que el ECG del caso 2 es MUY BONITO Y MUY FEO a la vez.
Ya trataremos mas adelanta el diagnóstico del IAM en presencia de bloqueo de rama, que ya se que esto da muchos quebraderos de cabeza.
1. Galiuto L(1), Barchetta S, Paladini S, Lanza G, Rebuzzi AG, Marzilli M, Crea F. Functional and structural correlates of persistent ST elevation after acute myocardial infarction successfully treated by percutaneous coronary intervention. Heart. 2007 Nov;93(11):1376-80. Epub 2007 Feb 19.



